| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 胃癌 | 二次治療 | 第3相 | 全生存期間 | 国内 | あり |
試験名 :WJOG 4007
レジメン:パクリタキセル vs イリノテカン
登録期間:2007年8月〜2010年8月
背景
JCOG9912試験やSPIRITS試験などの結果に基づいて、本邦における進行胃癌に対する標準的一次治療はS-1+シスプラチン療法となっているが、これらの試験が実施された当時、明確な生存延長を示すデータが存在していなかったにもかかわらず、70%を超える症例が二次化学療法を受けていた。
二次化学療法については多くの第2相試験が行われている。タキサン系薬剤に関しては、パクリタキセル(210mg/m2)とドセタキセル(60mg/m2)の3週毎投与法ではGrade 3-4の好中球数減少が高頻度(37~88%)であったのに対し、パクリタキセル毎週投与法(80mg/m2)では低頻度であった(3~32%)。奏効割合や無増悪生存期間はいずれの投与法も同様の結果であり、パクリタキセル毎週投与法の生存期間中央値は5~6.9ヶ月と報告されている。一方、イリノテカン隔週投与(150mg/m2)はパクリタキセル毎週投与法より高度な有害事象が生じるものの、生存期間中央値は8~10ヶ月とされている。
本試験はフッ化ピリミジン系+白金製剤に不応となった進行胃癌に対する二次治療としてのパクリタキセルとイリノテカンを比較検討する第3相試験として実施された。
二次化学療法については多くの第2相試験が行われている。タキサン系薬剤に関しては、パクリタキセル(210mg/m2)とドセタキセル(60mg/m2)の3週毎投与法ではGrade 3-4の好中球数減少が高頻度(37~88%)であったのに対し、パクリタキセル毎週投与法(80mg/m2)では低頻度であった(3~32%)。奏効割合や無増悪生存期間はいずれの投与法も同様の結果であり、パクリタキセル毎週投与法の生存期間中央値は5~6.9ヶ月と報告されている。一方、イリノテカン隔週投与(150mg/m2)はパクリタキセル毎週投与法より高度な有害事象が生じるものの、生存期間中央値は8~10ヶ月とされている。
本試験はフッ化ピリミジン系+白金製剤に不応となった進行胃癌に対する二次治療としてのパクリタキセルとイリノテカンを比較検討する第3相試験として実施された。
シェーマ
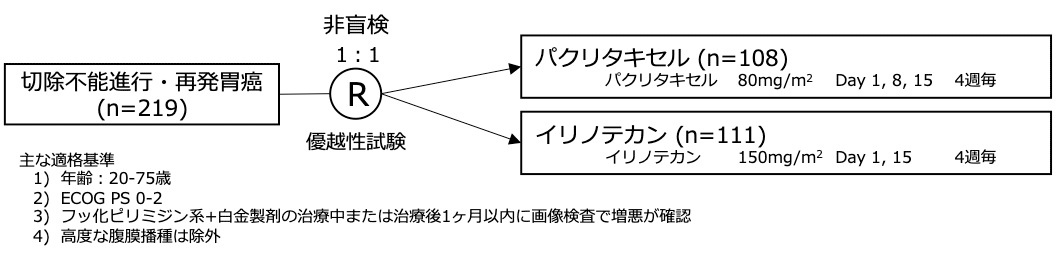
統計学的事項
主要評価項目:全生存期間
過去に報告された第2相試験の結果に加え、筆者らの見解(パクリタキセル後のイリノテカンは腹膜播種の増悪により投与が困難と想定)を合わせて、本試験はパクリタキセル群の生存期間中央値を5ヶ月、イリノテカン群の生存期間中央値を7.5ヶ月と推定した。よって、本試験はパクリタキセルを対照群としてイリノテカンの全生存期間のハザード比が0.67となることを検証する優越性試験として設計され、検出力80%、両側α=0.05として、220例の登録が必要と設定された。試験結果:
- 2007年8月〜2010年8月の間に日本国内37施設より223例が登録され、パクリタキセル群に111例、イリノテカン群に112例が割り付けられた。
- 前治療がフッ化ピリミジン単独療法(パクリタキセル群 2例/イリノテカン群 1例)と画像検査で増悪なし(パクリタキセル群 1例)の4例は適格基準を満たさず、パクリタキセル群108例とイリノテカン群111例を解析対象とした。
- 無作為割付後にパクリタキセル群 3例とイリノテカン群 2例は規定の治療が行われなかったため、安全性解析対象はパクリタキセル群 108例/イリノテカン群 110例となった。
- 観察期間中央値は17.6ヶ月であった。
1. 患者背景
- 患者背景は両群間でバランスがとれていた。
2. 全生存期間(主要評価項目)
| 中央値 | 95% 信頼区間 | HR 1.13 (95%C.I. 0.86-1.49) p=0.38 |
|
| パクリタキセル | 9.5ヶ月 | 8.4-10.7 | |
| イリノテカン | 8.4ヶ月 | 7.6-9.8 |
3. 無増悪生存期間
| 中央値 | 95% 信頼区間 | HR 1.14 (95%C.I. 0.88-1.49) P=0.33 |
|
| パクリタキセル | 3.6ヶ月 | 3.3-3.8 | |
| イリノテカン | 2.3ヶ月 | 2.2-3.1 |
4. 奏効割合
| 標的病変あり | 奏効割合 | p=0.24 | |
| パクリタキセル | N=91 | 20.9% | |
| イリノテカン | N=88 | 13.6% |
5. 投与状況
- 投与回数中央値(範囲):パクリタキセル群 11.5回(1-146)/イリノテカン群 4.5回(1-39)
- 治療中止理由の内訳:病勢進行(86.7%)/有害事象(7.3%)/同意撤回(3.2%)/その他(2.8%)
- 有害事象による治療中止:パクリタキセル群 5.6%/イリノテカン群 9.1%
6. 有害事象 (CTCAE ver.3.0)
| N (%) | パクリタキセル n=108 | イリノテカン n=110 | ||
|---|---|---|---|---|
| 全Grade | Grade 3-4 | 全Grade | Grade 3-4 | |
| 白血球減少 | 88 (81.4) | 22 (20.4) | 76 (69.4) | 21 (19.1) |
| 好中球数減少 | 85 (78.7) | 31 (28.7) | 77 (70.0) | 43 (39.1) |
| 貧血 | 69 (63.9) | 23 (21.3) | 84 (76.4) | 33 (30.0) |
| 血小板数減少 | 6 (5.6) | 1 (0.9) | 15 (13.6) | 2 (1.8) |
| 発熱性好中球減少症 | 3 (2.8) | 3 (2.8) | 10 (9.1) | 10 (9.1) |
| 悪心 | 33 (30.6) | 2 (1.9) | 61 (55.5) | 5 (4.5) |
| 食欲不振 | 50 (46.3) | 8 (7.4) | 78 (70.1) | 19 (17.3) |
| 下痢 | 21 (19.4) | 1 (0.9) | 49 (44.5) | 5 (4.5) |
| 末梢性感覚ニューロパチー | 62 (57.4) | 8 (7.4) | 2 (1.8) | 0 (0) |
| 血中ビリルビン増加 | 10 (9.3) | 3 (2.8) | 21 (19.1) | 4 (3.6) |
| 低ナトリウム血症 | 21 (19.4) | 4 (3.7) | 35 (31.8) | 17 (15.5) |
| 治療関連死亡 | 0 (0) | 2 (1.8) | ||
- 最終投与日から30日以内の死亡:パクリタキセル群 3例(2.7%)/イリノテカン群 4例(3.6%)
- 治療関連死亡:パクリタキセル群では認めなかったが、イリノテカン群で2例(1.8%)に認めた(重症肺炎 1例/胃穿孔 1例)。
7. 後治療
| N (%) | パクリタキセル | イリノテカン | p値 |
|---|---|---|---|
| 三次化学療法施行 イリノテカン タキサン |
97 (89.8) 81 (75.0) — |
80 (72.1) — 67 (60.4) |
0.001 — — |
| 三次化学療法以降:全て イリノテカン タキサン |
87 (80.6) — |
— 75 (67.6) |
— |
8. 生存期間に関するサブグループ解析
- ほぼ全てのサブグループで、パクリタキセルの生存期間がやや良好であったが、統計学的な有意差は認めなかった。
| 症例数 | ハザード比 | 95%信頼区間 | ||
|---|---|---|---|---|
| 全症例 | 219 | 1.13 | 0.86-1.49 | |
| 年齢 | 65歳未満 65歳以上 |
109 110 |
1.36 0.97 |
0.92-2.01 0.65-1.44 |
| 性別 | 男性 女性 |
171 48 |
1.08 1.38 |
0.79-1.48 0.76-2.49 |
| ECOG PS | 0-1 2 |
211 8 |
1.12 7.27 |
0.85-1.49 0.79-66.6 |
| 胃切除歴 | あり なし |
60 159 |
1.05 1.24 |
0.61-1.80 0.90-1.71 |
| 組織型 | Intestinal(腸型) Diffuse(びまん型) |
108 110 |
1.15 1.11 |
0.77-1.71 0.75-1.63 |
| 測定可能病変 | あり なし |
183 36 |
1.19 0.91 |
0.88-1.61 0.46-1.81 |
| 腹膜播種 | あり なし |
56 163 |
1.31 1.07 |
0.76-2.28 0.77-1.48 |
| 転移臓器個数 | 0-1臓器 2臓器以上 |
121 98 |
0.91 1.64 |
0.62-1.33 1.08-2.49 |
- 探索的解析では二次化学療法以降にイリノテカンとパクリタキセル両剤を使用した症例で解析を行ったが、統計学的有意差は認めなかった。
| パクリタキセル | イリノテカン | |
|---|---|---|
| 生存期間中央値 | 10.1ヶ月 | 10.1ヶ月 |
HR 0.96 (95%C.I. 0.69-1.32), p=0.96
結語
本試験の結果、パクリタキセルとイリノテカンは進行胃癌に対する二次化学療法としていずれも選択可能なレジメンと考えらえた。各レジメンの毒性の特徴と投与間隔の違いが治療方針を決定する上で参考になると考えられた。
執筆:九州大学大学院 消化器・総合外科 助教 中島 雄一郎 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生