| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 胃癌 | 二次治療以降 | 第2相 | 全奏効割合 | 日本 | あり |
試験名 :JFMC45-1102
レジメン:パクリタキセル+トラスツズマブ
登録期間:2011年9月〜2012年3月
背景
無作為化比較試験(a,b)により、イリノテカン(IRI)またはドセタキセル(DOC)単剤療法による二次化学療法が、一次化学療法不応後の進行胃癌患者に延命効果をもたらすことができることが示された。WJOG 4007試験では、パクリタキセル(PTX)がIRIと同等の有効性を示すことが示されたため、PTXは進行胃癌の二次化学療法において最も一般的なレジメンの1つとして利用されている。
化学療法未施行例を対象として実施された国際共同無作為化比較第3相試験であるToGA試験において、化学療法(カペシタビン〔Cape〕/フルオロウラシル+シスプラチン〔CDDP〕)+トラスツズマブ併用療法が、HER2陽性患者の全生存期間を延長することを示した。ただし、全ての患者が一次化学療法でトラスツズマブを併用されるわけではなく、さらに、術後補助化学療法としてのトラスツズマブの有用性は確立されていない。したがって、HER2陽性の進行胃癌または早期再発胃癌症例に対する二次化学療法としてのトラスツズマブの有効性を評価する必要がある。
以上より、既治療HER2陽性胃癌でトラスツズマブ未治療症例に対するPTX+トラスツズマブ療法の有効性と安全性を検証することとした。
化学療法未施行例を対象として実施された国際共同無作為化比較第3相試験であるToGA試験において、化学療法(カペシタビン〔Cape〕/フルオロウラシル+シスプラチン〔CDDP〕)+トラスツズマブ併用療法が、HER2陽性患者の全生存期間を延長することを示した。ただし、全ての患者が一次化学療法でトラスツズマブを併用されるわけではなく、さらに、術後補助化学療法としてのトラスツズマブの有用性は確立されていない。したがって、HER2陽性の進行胃癌または早期再発胃癌症例に対する二次化学療法としてのトラスツズマブの有効性を評価する必要がある。
以上より、既治療HER2陽性胃癌でトラスツズマブ未治療症例に対するPTX+トラスツズマブ療法の有効性と安全性を検証することとした。
シェーマ
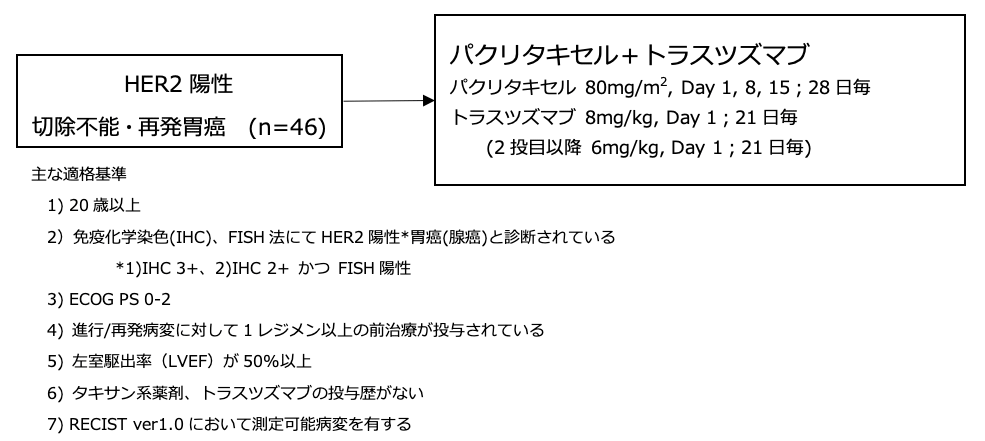
統計学的事項
主要評価項目:全奏効割合(最良効果)
副次評価項目:無増悪生存期間、治療成功期間、全生存期間、有害事象
進行/再発胃癌において、二次治療以降のタキサン系薬剤単剤療法における全奏効割合は15-20%と報告されていることから、閾値奏効割合を15%と設定し、トラスツズマブ併用による上乗せ効果を15%と想定。検出力80%、片側 α=0.05として、必要症例数を47例と設定した。試験結果:
- 2011年9月〜2012年3月までの期間に35施設から47人が登録された。
- 臓器機能より1例が不適格とされ、46例が最終解析の対象となった。
- 登録症例のHER2 statusは、免疫化学染色(IHC) 3+/FISH陽性:9例(20%)、IHC 3+/FISH未検:24例(52%)、IHC 2+/FISH陽性:13例(28%)であった。前治療レジメン数は1レジメン:39例(85%)、2レジメン:5例(11%)、3レジメン:2例(4%)であった。
- データカットオフ時点(2013年4月15日)で治療継続中が6例、治療中止は40例であった(中止例の治療期間中央値:128.5日, 範囲:4-486日)。治療中止理由の内訳は、病勢進行:36例(78%)、有害事象による死亡:2例(4%)、有害事象に基づく主治医判断:1例(2%)、28日を超えた治療延期:1例(2%)であった。
- PTXの投与状況:休薬:8例、投与延期:13例、減量:15例
- トラスツズマブの投与状況:休薬/減量:0例
- 試験治療開始後60日以内の中止:病勢進行:3例、有害事象:2例、有害事象に基づく主治医判断:1例
1. 全奏効割合(最良効果)(主要評価項目)
| CR | PR | SD | PD | NE | 全奏効割合 | 95%信頼区間 | ||
|---|---|---|---|---|---|---|---|---|
| N=46 | N (%) |
1 (2.2) |
16 (34.8) |
21 (45.7) |
6 (13.0) |
2 (4.3) |
17 37% |
23-52 |
- NEの2例は初回/2回目の評価前に死亡した
2. 無増悪生存期間
| 中央値 | (範囲) | 95%信頼区間 | |
|---|---|---|---|
| N=46 | 5.1ヶ月 | (0.4-18.8) | 3.8-6.5 |
3. 治療成功期間
| 中央値 | (範囲) | 95%信頼区間 | |
|---|---|---|---|
| N=46 | 5.1ヶ月 | (0.4-18.8) | 3.7-6.5 |
4. 全生存期間
| 中央値 | (範囲) | 95%信頼区間 | |
|---|---|---|---|
| N=46 | 17.1ヶ月 | (0.4-18.8) | 13.5-18.6 |
5. サブグループ別の治療効果
治療効果について、疾患状況(切除不能・進行/再発)、CDDP投与歴の有無、組織型(Lauren分類:腸型[Intestinal]/びまん型[Diffuse]/その他)に分けて解析した。
| 全奏効割合 | 生存期間中央値 | 無増悪生存期間中央値 | |
|---|---|---|---|
| 病期 切除不能・進行 (n=24) 再発 (n=22) p値 |
25% 50% 0.126 |
11.68 ヶ月 18.65 ヶ月 0.0008 |
3.92 ヶ月 6.67 ヶ月 0.0137 |
| CDDP投与歴 なし (n=22) あり (n=24) p値 |
36 38 1.000 |
16.81 16.08 0.4134 |
5.09 4.53 0.6807 |
| 組織型 (Lauren) 腸型[Intestinal] (n=37) びまん型[Diffuse]/その他 (n=9) p値 |
43 11 0.167 |
16.81 17.13 0.40 |
5.07 5.11 0.34 |
- 再発例の全生存期間、無増悪生存期間は、切除不能・進行例と比較して有意に良好な結果であった。
6. 有害事象 (CTCAE v4.0) [10%以上の事象]
| N (%) | Grade 1-5 | Grade≥3 |
|---|---|---|
| N (%) | N (%) | |
| 白血球減少 | 35 (76.1) | 8 (17.4) |
| 好中球数減少 | 31 (67.4) | 15 (32.6) |
| 血小板数減少 | 5 (10.9) | 0 (0.0) |
| AST増加 | 22 (47.8) | 3 (6.5) |
| ALT増加 | 18 (39.1) | 2 (4.3) |
| ALP増加 | 22 (47.8) | 0 (0.0) |
| 低ナトリウム血症 | 12 (26.1) | 1 (2.2) |
| 低カリウム血症 | 5 (10.9) | 1 (2.2) |
| 高カリウム血症 | 16 (34.8) | 0 (0.0) |
| クレアチニン増加 | 8 (17.4) | 0 (0.0) |
| 低アルブミン血症 | 27 (58.7) | 4 (8.7) |
| 貧血 | 23 (50.0) | 7 (15.2) |
| 食欲不振 | 20 (43.5) | 2 (4.3) |
| 悪心 | 15 (32.6) | 1 (2.2) |
| 口腔粘膜炎 | 8 (17.4) | 0 (0.0) |
| 腹痛 | 5 (10.9) | 0 (0.0) |
| 末梢性運動ニューロパチー | 8 (17.4) | 0 (0.0) |
| 末梢性感覚ニューロパチー | 29 (63.0) | 3 (6.5) |
| 疲労 | 28 (60.9) | 2 (4.3) |
| 四肢浮腫 | 10 (21.7) | 0 (0.0) |
- 心毒性や蓄積性の毒性は認められなかった。
- 有害事象による死亡例が3例認められた。①意識障害, 5日目(因果関係:不明)、②肺線維症, 45日目(因果関係:明らかにあり:PTX and/or トラスツズマブ)、③原疾患の急激な増悪, 治療中止後22日目(因果関係:なし)
- 高頻度に発生したGrade 3/4の有害事象:好中球数減少(n=15, 32.6%)、白血球減少(n=8, 17.4%)、貧血(n=7, 15.2%)、低アルブミン血症(n=6, 8.7%)であった。
7. サブグループ別の有害事象
Grade 3以上の有害事象の発現頻度について、疾患状況(切除不能・進行/再発)、CDDP投与歴の有無、組織型(Lauren分類:腸型[Intestinal]/びまん型[Diffuse]/その他)に分けて解析した。
| Grade 3以上の有害事象 | |
|---|---|
| 病期 切除不能・進行 (n=24) 再発 (n=22) |
n=16, 66.7% n=11, 50% |
| CDDP投与歴 なし (n=22) あり (n=24) |
N=14, 63.6% N=13, 54.2% |
| 組織型 (Lauren) 腸型[Intestinal] (n=37) びまん型[Diffuse]/その他 (n=9) |
N=23, 62.2% N=4, 44.4% |
8. 後治療
| レジメン | N | 治療期間中央値 (日) | 範囲 |
|---|---|---|---|
| IRI | 16 | 43 | 1–218 |
| 放射線療法 | 6 | 14 | 1–38 |
| IRI+CDDP | 4 | 113 | 57–275 |
| DOC | 4 | 25 | 21–43 |
| Cape+トラスツズマブ | 3 | 64 | 22–162 |
| 外科治療 | 3 | 1 | 1-1 |
| トラスツズマブ | 3 | 64 | 1–189 |
| PTX+トラスツズマブ | 3 | 15 | 15–50 |
| IRI+トラスツズマブ | 2 | 155.5 | 22–289 |
| Cape+CDDP+トラスツズマブ | 2 | 137 | 98–176 |
| IRI+マイトマイシンC | 1 | 1 | ― |
| IRI+S-1 | 1 | 55 | ― |
| Cape | 1 | 148 | ― |
| Cape+CDDP+IRI | 1 | 163 | ― |
| Cape+IRI+トラスツズマブ | 1 | 55 | ― |
| PTX | 1 | 36 | ― |
| S-1 | 1 | 56 | ― |
| S-1+CDDP | 1 | 98 | ― |
| S-1+トラスツズマブ | 1 | 105 | ― |
- 病勢進行に続く後治療として、IRI単剤療法(n=16)、放射線療法(n=6)などが実施されていた。病勢進行後のトラスツズマブ継続投与は9症例で実施されており、更に14症例ではその後の治療ラインにてトラスツズマブの再導入がなされていた。
結語
既治療かつPTX/トラスツズマブの治療歴のない切除不能HER2陽性胃癌に対するPTX+トラスツズマブ併用療法は、良好な治療効果と忍容性を示したことから、有望な治療選択肢の一つとなる可能性が示唆された。
執筆:大阪医療センター 消化器内科 医師 長谷川 裕子 先生
監修:近畿大学医学部 内科学教室 腫瘍内科部門 医学部講師 川上 尚人 先生
監修:近畿大学医学部 内科学教室 腫瘍内科部門 医学部講師 川上 尚人 先生